科研进展
云南大学于黎研究员和胡靖扬研究员报道中华穿山甲的博物馆基因组学研究成果
转载自微信公众号:动物进化研究课题组
近日,团队于黎研究员和胡靖扬研究员,继发表树穿山甲系统地理基因组学研究成果的基础上(图1),在中华穿山甲的博物馆基因组学研究中再次取得突破。

图1、树穿山甲系统地理基因组学研究成果,Molecular Biology and Evolution封面文章。
团队从博物馆中,收集获取了22份跨越超过60个世代的中华穿山甲的基因组数据,通过博物馆基因组学研究揭示了极度濒危的中国穿山甲的动态遗传后果和灭绝风险,为中华穿山甲种群持续下降的复杂基因组遗传后果提供了新的见解。研究结果以“Pangolin museum genomics reveal the dynamic genetic consequences and extinction risk of the critically endangered Chinese pangolin”为题,于4月9日发表在国际期刊Molecular Biology and Evolution(JCR和中科院双一区,5年影响影子11.9)上。原文链接:https://doi.org/10.1093/molbev/msag099
由于人类活动的影响,再加上非法捕猎和走私的日益严重,许多野生动物的种群数量急剧减少,甚至走向灭绝。因此,开展长期的基因组侵蚀研究,为制定保护策略提供科学依据,就变得格外重要。虽然科学家可以通过分析古DNA、历史或博物馆标本的基因组序列,了解这些物种不同世代间遗传上的变化,但往往因为样本数量太少,很难深入弄清种群长期衰退的完整过程。这也说明,我们需要开展长期连续时间尺度下的研究,才能更好地理解在持续灭绝压力下,种群是如何一步步衰退和如何维持存续?
中华穿山甲(学名:Manis pentadactyla)因为过去被过度捕杀和利用,已被IUCN列为极度濒危物种,同时也是我国的国家一级保护野生动物(图2)。该物种历史上和现在都仅分布于中国南部、东南亚北部和南亚北部。中国穿山甲具有缓慢的生活史策略,其繁殖率低(通常每胎仅产一仔,雌性每年产仔一次或更少),扩散能力有限。这些特征,再加上其对蚂蚁的专一性食性以及对栖息地破碎化的脆弱性,导致其种群恢复缓慢,灭绝风险更高。

图2、中华穿山甲图片。图片来自缤纷自然。
20 世纪 60 年代,中国穿山甲的种群数量约为 80 万只,此后由于持续不断的偷猎和非法交易,其数量一直在持续下降。20 世纪 90 年代末,其种群数量估计约为 6.4 万只,到 2020 年估计约为 1.6 万只。这些统计数据表明,在两个时间段内数量大幅下降:1980 年代至 1990 年代急剧减少约 90%(约减少 736,000 只),2000年至 2020 年又进一步减少约 75%(约减少 48,000 只)。总体而言,中华穿山甲的数量自 20 世纪 60 年代以来持续下降,经历了两个严重程度和速度不同的时期。我们将 1979 年之前至 1980 年至 1999 年定义为数量下降的第一阶段,1980 年至 1999 年至 2000年及以后定义为第二阶段。尽管这种严重的种群缩减持续了 60 多年,超过 60 个世代(穿山甲的代时为一年),但是这种长期持续的种群下降,对它的基因组造成了哪些遗传后果的动态影响,以及由此带来的灭绝风险有多大,我们至今还了解得不够深入。因此,我们整合了来自博物馆和现代中国穿山甲样本的不同时间的基因组学数据,跨越种群持续下降的不同时期,探索人类活动对遗传侵蚀的影响。基于对228个穿山甲基因组(133个新测序)的分析,本研究为种群持续下降的基因组遗产提供了新的见解,阐明了人类活动对遗传侵蚀的影响,并为有针对性的保护策略提供了科学框架。
基于系统发育分析、混合分析和主成分分析(PCA),将所有个体划分为5个种群,其中4个是已经报道的种群(青藏高原南部、中南半岛种群、中国西南部和中国南部)(图3)。与之前的研究相比,通过整合更多来自青藏高原南部的新生成样本,我们的种群结构分析显示了一个重要的发现。具体来说,青藏高原南部种群进一步分化为两个不同的亚种群:尼泊尔亚种群和中缅亚种群(图1B-1D)。值得注意的是,中国西南地区和华南地区的人口样本涵盖了所有三个时期(1979年前、1980-1999年和2000年后)的样品。考虑到青藏高原南部和中南半岛种群的样本是最近没收的,没有历史标本,这两个种群不包括在种群历史动态趋势和遗传后果的分析中。
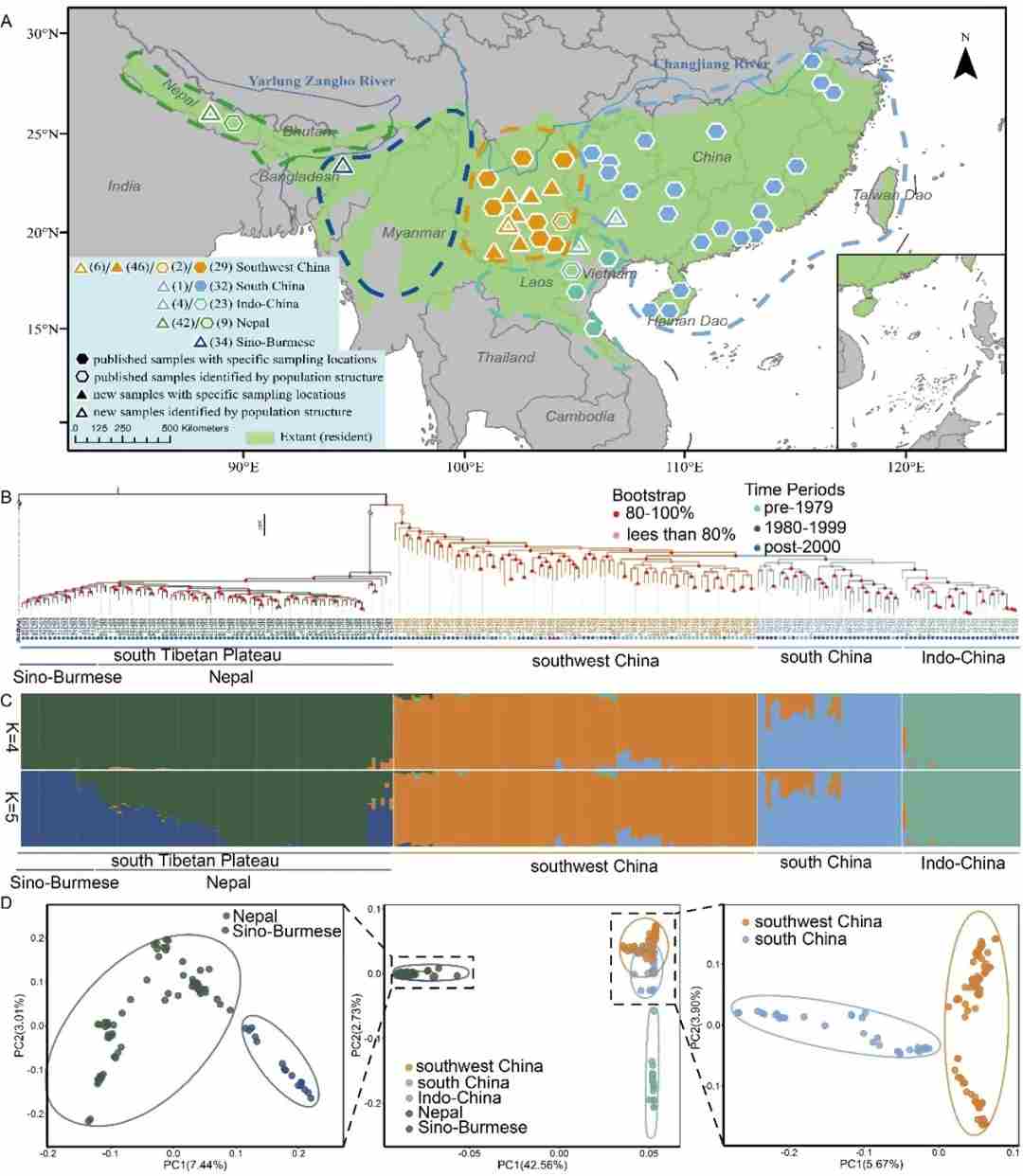
图3、中国穿山甲博物馆标本和当代标本的取样信息和种群结构。
(A)样本信息。共获取了 228 个中华穿山甲的基因组数据,其中包括 133 个新获得的样本和 95 个已发表的样本。已知来源的样本在地图上有所显示。三角形代表新样本,五边形代表已发表样本。具有特定采样地点的样本为实心图形,而通过种群结构确定来源地点的样本为空闲形状。不同的颜色代表不同的遗传群体。现存中国穿山甲的分布范围来自国际自然保护联盟(IUCN)。 (B)基于最大似然(ML)系统发育树的种群结构结果。在树中使用不同颜色编码的圆圈列出了支持率的置信值和采样时间段的信息。置信值为 80%-100% 和 <80% 的分支用红色和橙色显示。1979 年之前、1980 年至1999 年以及 2000 年之后的样本的时间段分别用绿色、紫色和蓝色样本名称表示。 (C)K 值在 4 至 5 之间的混合结果,并支持了五个祖先群体(K=5)。 (D)中国穿山甲的主成分分析(PCA)。深绿色、深蓝色、橙色、浅蓝色和浅绿色分别代表了中国穿山甲的中缅种群、尼泊尔种群、中国西南部种群、中国南部种群以及中南半岛种群。
本研究的分析揭示了导致种群持续下降的遗传复杂性的新见解。我们通过基因检测证实,中国分布的穿山甲自 20 世纪 60 年代以来一直在减少,其间经历了两次主要的种群减少(1980 年至 1999 年以及2000 年以后)。第一次显著的减少(1980 年至 1999年)可能是由于大规模的商业捕猎所致,这种捕猎受到对消费和药用需求的强烈推动,当时缺乏法律保护和广泛的保护意识。尽管中华穿山甲于 1995 年被列入《濒危野生动植物种国际贸易公约》附录 II 中,1997 年被国际自然保护联盟列为濒危物种,并在中国被列为二级保护物种,但这些保护措施却因黑市价格的飙升以及非法贸易带来的巨额利润而受到破坏。因此,尽管多次颁布禁令,但偷猎和走私行为仍持续存在,导致种群数量再次大幅下降,尽管下降速度较之前有所放缓。然而,在这两个时间段内,中国西南部和南部的种群下降程度有所不同(图4A)。西南部种群在 1980 年至 1999 年期间经历了最为显著的下降,而南部种群在 2000 年以后则呈现出更为明显的减少趋势。与此同时,随着种群数量下降程度的加剧,遗传后果的动态变化也愈发明显。在 1980 年至 1999 年期间,中国西南地区的种群表现出更大的遗传多样性损失、更高的近亲繁殖水平以及更显著的遗传负荷累积,而这一时期的人口减少程度比 2000 年以后更为严重。在 2000 年以后的时期里,中国南方地区的种群在人口减少程度更严重的情况下也表现出了更负面的遗传后果(图4B 至 4F)。我们的研究结果表明,在 1980 年至 1999 年期间,中国西南地区的种群减少更为严重,这可能是由于当时的人类活动(如狩猎和栖息地破碎化)以及对中国西南地区分布的自然保护区管理不善所导致的。此外,在 2000 年以后的时期里,中国南方地区的种群出现了更严重的种群减少,这进一步支持了人类人口数量显著增加和土地使用加剧,可能是导致穿山甲种群萎缩以及中国南方地区更严重遗传后果的主要原因。我们的研究结果表明,在不同种群内部,持续的种群下降驱动遗传后果的持续衰退,种群数量下降的严重程度与负面遗传后果的影响直接正相关——比如基因多样性减少、近亲繁殖增多、有害基因累积,对应的灭绝风险也会越高(图2)。但令人意外的是,在不同地区的中华穿山甲种群间,衰退最严重的种群(比如中国西南地区的中华穿山甲),基因组受到的相对影响,反而比衰退程度较轻的种群(比如中国华南地区的中华穿山甲)要小,这可能预示着不同种群衰退前的原始规模(也就是历史有效种群大小),对其基因组遗传后果的影响更大(图 4)。
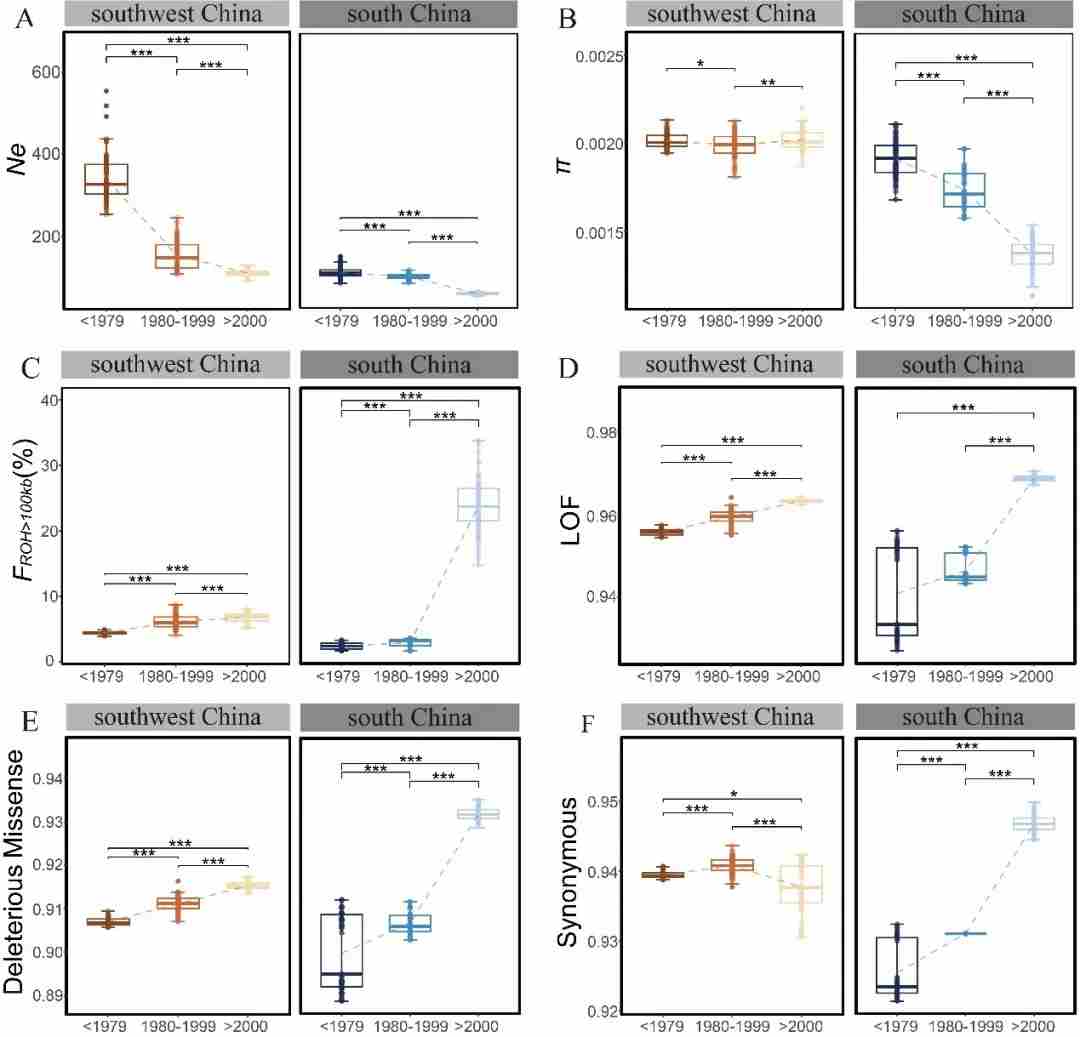
图 4、中国西南部和南部穿山甲种群的动态遗传学影响。(A)有效种群规模(Ne)进行了 100 次估算,(B)核苷酸多样性(π),(C)近交系数(FROH>100kb),(D)功能丧失(LOF)突变的遗传负荷,(E)有害错义突变的遗传负荷,以及(F)同义突变的遗传负荷。虚线表示中位数的趋势。每个遗传影响因素都进行了 100 次抽样。所有结果均使用Wilcoxon rank-sum检验方法进行显著性测试。***、** 和 * 分别代表 P 值小于 0.001、小于 0.01 和小于0.05。
此外,模拟结果表明,在中国穿山甲西南部和南部种群中,随着承载能力的降低,其灭绝概率会随着种群数量持续下降的情况而逐渐上升。相反,如果采取积极有效的保护措施,以促进未来 1000 年内种群规模的增长,适应能力则会随着承载能力的增加而恢复(图 5)。这些发现强调,维持或增加种群规模是小而濒危种群长期生存能力的关键决定因素。种群数量的减少会导致遗传多样性降低和遗传负担增加,这会削弱适应能力和种群的恢复能力,从而提高灭绝风险。相比之下,种群增长可以通过扩大有效种群规模、减缓遗传漂变、清除有害突变以及促进适应能力的恢复来缓解遗传限制。尽管当前的种群增长趋势令人担忧,但本研究也表明,有针对性的、基于科学的保护干预措施能够有效地改变这些趋势。因此,必须加强和扩大现有保护区的管理,加强与执法部门的合作,并加大打击偷猎和非法交易的力度。此外,应在关键地区实施栖息地恢复计划,以科学方式缓解栖息地破碎化问题。这些措施应得到加强的基础研究的支持,这些研究涉及穿山甲的生态学、疾病和繁殖生物学等方面,这将有助于推进圈养繁殖计划并促进种群恢复。
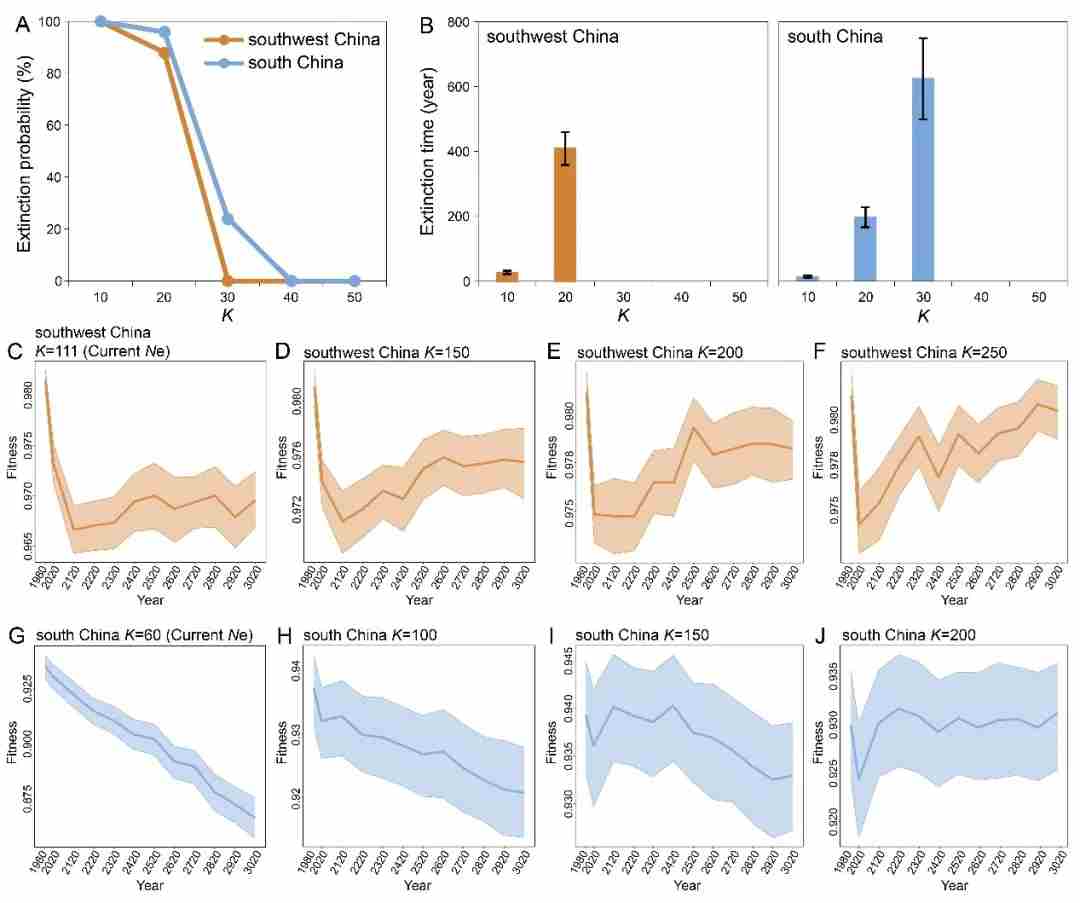
图 5、对中国西南部和南部中华穿山甲种群的Non-Wright–Fisher的未来演化模拟分析。(A)灭绝概率。横轴表示接下来 1000 年的不同承载能力(K)。纵轴表示 100 次模拟中的灭绝概率。(B)灭绝时间。柱状图的上下限为标准误差线。(C)至(F)中国西南部种群在 K = 当前有效群体大小(C)、K = 150(D)、K = 200(E)和 K = 250(F)时的适合度。如果 K 值增加 150、200 和 250,适合度将分别恢复0.15%、0.34% 和 0.64%。(G)至(J)中国南部种群在 K = 当前有效群体大小(G)、K = 100(H)、K = 150(I)和 K = 200(J)时的适合度。适合度的下降程度从 K = 100 时的 1.79% 降至 K = 150 时的0.34%,在 K = 200 时达到平衡(无变化)。
值得注意的是,与西南部的中华穿山甲种群相比,南部种群具有更小的有效种群规模、更差的遗传后果以及更高的灭绝风险(图4 和图 5)。因此,保护南部中华穿山甲种群是当务之急。2020 年,中国政府在南部的中国广东省建立了中国穿山甲保护与研究中心,并将该物种列为国家一级保护动物。这些举措旨在加强对中国穿山甲的保护措施,并促进南部中华穿山甲种群的恢复和增长。然而,保护资源在南部(投入较大)和西南部(投入较小)地区的分配不均可能会通过不同的调查强度而非实际的生态偏好导致不准确的分布模式。从文献资料、访谈以及实地观察中获得的多条证据(2010 年至 2023 年)表明,与华南地区的种群相比,西南地区的种群记录较少。然而,我们从西南地区采集的新样本(2010 年至 2024 年期间),主要来自非法交易活动。这表明西南地区的种群可能与缅甸等跨境地区有关。中国与缅甸边境沿线的调查数据稀缺,可能导致对该种群状况的评估不全面。因此,未来的保护策略不仅应持续加强对已记录的华南种群的有力保护,还应扩大工作范围,对物种的整个分布区域进行全面调查,尤其要重视西南地区的种群,并加强跨区域保护方面的国际合作。
总之,本研究通过将来自博物馆和现代中华穿山甲样本的时间动态基因组学数据相结合,我们揭示了人类活动对基因组遗传后果的动态变化影响是直接且一致的,但复杂之处在于多个因素(历史的自然选择强度、种群数量的减少程度、种群减少的持续时间和严重程度以及个体的响应或适应能力)相互作用并相互叠加以产生结果的过程。尽管种群间的遗传后果与种群减少的严重程度直接相关,但种群内部的差异主要由历史的有效种群规模决定,而非种群减少的强度。至关重要的是,中国南方种群显示严重降低遗传多样性、较高的近交程度和更大灭绝风险,比中国西南部种群更为突出,这要求优先进行保护。这项工作为基于科学的开展极度濒危物种的保护建立了框架。
团队胡靖扬研究员为论文的第一作者和共同通讯作者,于黎研究员为论文的末位通讯作者,实验室硕士研究生蒋宇(硕士二年级)参与了该工作的数据分析。昆明动物研究所动物自然历史博物馆李松老师、昆明动物研究所遗传资源与进化国家重点实验室尹婷婷老师参与了样品收集和整理。本研究获国家自然科学基金(32470527和32160130)、云南省兴滇英才支持计划、云南省基础研究计划(202301AT070185)、云南省科技厅-云南大学联合基金(202401BF070001-018)以及中央引导地方科技发展资金(202407AB110004)支持。感谢中国科学院野生生物种质库动物分库对样品收集工作的大力支持。感谢领克生物(昆明)有限公司提供的测序服务,感谢合肥曙光先进计算中心提供的计算服务。
发布者:
发布日期:2026-04-10
来源:动物进化研究课题组
